こちらでは酸化ストレスマーカーの技術情報、学術情報をご紹介しております。皆様のご研究に役立てて頂ければ
幸いです。
またよろしければ、学会や論文等で発表された内容をご紹介頂ければ大変ありがたく思います。
ご質問・コメントなどお気軽にお送り頂けると助かります。
biotech@jaica.comまでお気軽にお知らせください。
対象となるマーカーも徐々に増やしていきたいと思います。どうぞよろしくお願い申し上げます。
弊社は本ホームページおよび製品、添付文書等を作成するにあたり細心の注意を払っておりますが、これらによる損害が万一発生した場合でも、
弊社は責を負いませんので予めご了承ください。また、製品の価格、仕様、試薬構成、測定手順等は、製造元の都合により予告無く変更される
場合があります。 |
|
| タンパク質過酸化物(AOPP)測定キット |
| No. |
【タイトル】 |
【内容】 |
| 1 |
Q:分光光度計でも測定できますか? |
A:測定可能ですが、必要なサンプル量と試薬液量にご注意ください。 |
| 2 |
Q:EDTA血漿以外にも適用できますか? |
A:ヘパリン血漿や血清サンプルでも測定できると考えられますが、EDTA血漿の場合と
数値が異なる可能性があります。また、実験動物につきましては、ラットでの測定例があるようです。 |
| 3 |
Q:基準値はありますか? |
A:研究用試薬であるため基本的には参考値/基準値の設定はありませんが、下記のような
数値が報告されております。研究施設や母集団の設定によって数値が大きく異なる場合がありますのでご注意ください。
血漿測定値:透析患者149±41μmol/L (Circulation 106, p2212-2217,2002)
血清測定値:透析患者144.3μmol/L、健常者89.2μmol/L(Nephrol Dial Transplant 18, p2577-2581, 2003) |
| 4 |
Q:コントロールの濃度を教えてください。 |
A:商品に同梱の「Produkt Spezifikation」(A4サイズ1枚)にコントロールの調製方法と
濃度が掲載されております。 |
| 5 |
Q:サンプルは凍結保存できますか? |
A:凍結保存した新鮮EDTA血漿でも測定可能です。凍結前に比べ凍結血漿のAOPPは
若干高くなる可能性があります。投与前後など比較試験をされる場合には、サンプル保存条件を統一することをお奨めします。
尚、数回凍結融解しても測定値への影響は軽微とされています。 |
| 6 |
尿中 AOPP測定法 |
本キットは尿サンプル中のAOPPを検出可能です。尿サンプルを測定する場合には、サンプル100μLに対し
サンプル希釈液200μLを混合します(1:3希釈)。血漿サンプルの場合と異なり、脱脂処理(DELIP試薬)は必要ありません。
補正法として、クレアチニン補正がよく用いられるようです。 |
| 7 |
Q:キットを誤って冷凍したのですが |
A:AOPP測定キットは、保管中に凍結した場合でも使用可能ですが、
試薬性能を十分発揮できるよう、保管条件(2〜8℃)を守るようにお願いいたします。 |
| 8 |
キット構成品の個別購入について |
製造元の在庫状況により、構成品を個別に入手できる場合があります。
価格、入手状況などにつきましては、個別にお問合せください。
(ご参考)AOPPキット用 脱脂試薬(DELIP): 税別20,000円/個 |
| 9 |
標準物質について |
標準物質の量が足りない場合には、同一ロットのバイアルを2本以上溶解し、
プールして使用してください。
標準物質のバイアルには、クロラミンTと蛋白質が含まれています。
尚、溶解後の標準物質は不安定であり、保存できません。 |
| 10 |
本キットの測定原理について(補足) |
本キットは主に340nmに吸収を持つ構造(例:ジチロシン)を検出すると考えられています。
ヒト血漿において、AOPP測定値はジチロシン測定値およびペントシジンと一定の相関を示すこと、一方、
過酸化脂質(TBARS)との相関性は低いことが報告されています。
ヒト血漿を対象とした解析では、分画分子量600kDa付近および80kDa付近にAOPP検出ピークが存在します。
|
| 11 |
本キットの仕様変更について |
2016年出荷分より、サンプルバッファー(50mL)、スタンダードバッファー(15mL)がなくなり、
アッセイバッファー(65mL)が追加されております。また、再構成の際の蒸留水の液量など、細かな変更があります。
ご使用の際には、必ず製品に同梱の使用説明書をご確認ください。
|
|
|
|
|
| 【参考文献】 |
| 1) |
Advanced oxidation protein products as a novel marker of oxidative stress in uremia.
Kidney Int. 49(5),p1304-1313 (1996)
Witko-Sarsat V, Friedlander M, Capeillere-Blandin C, Nguyen-Khoa T, Nguyen AT, Zingraff J, Jungers P, Descamps-Latscha B.
尿毒症患者血漿を対象にAOPPを測定した文献です。 |
| 2) |
Early prediction of IgA nephropathy progression: proteinuria and AOPP are strong prognostic markers.
Kidney Int. 66(4):1606-12. (2004)
Descamps-Latscha B, Witko-Sarsat V, Nguyen-Khoa T, Nguyen AT, Gausson V, Mothu N, Cardoso C, Noel LH, Guerin AP, London GM, Jungers P.
IgA腎症患者を対象にAOPPを測定した文献です。 |
| 3) |
Advanced oxidation protein products as risk factors for atherosclerotic cardiovascular events in nondiabetic predialysis patients.
Am J Kidney Dis. 45(1):39-47.(2005)
Descamps-Latscha B, Witko-Sarsat V, Nguyen-Khoa T, Nguyen AT, Gausson V, Mothu N, London GM, Jungers P.
uremic predialysis患者を対象に動脈硬化との関連性を調べた7年間の追跡調査です。心筋梗塞/脳梗塞発症群
(58±20μmol/L)は非発症群(42±14μmol/L)に比べ血漿AOPP濃度が有意に高値を示します。 |
| 4) |
Inflammation and oxidative stress markers by pentoxifylline treatment in rats with chronic renal failure and high sodium intake.
Arch Med Res. 38(1),p34-8.(2007)
Gallardo JM, de Carmen Prado-Uribe M, Amato D, Paniagua R.
ラットに対し5/6腎摘出術を行い慢性腎疾患モデルを作成。AOPP測定値はNaCl低摂取群(31.72μg/mL)、
中摂取群(45.89)、高摂取群(60.41)。血漿MDAには有意差なし。高摂取群へのpentoxifylline(PF)投与によりAOPP低下(49.83μg/mL)
|
| 5) |
Modulation of CD36 protein expression by AGEs and insulin in aortic VSMCs from
diabetic and non-diabetic rats.
Nutr Metab Cardiovasc Dis. 2006 Nov 24
de Oliveira Silva C, Delbosc S, Arais C, Monnier L, Cristol JP, Pares-Herbute N.
血漿AOPPは糖尿病ラット(GKラット)において対照ラットに比べ高値を示します。 |
| 6) |
Paraoxonase-1 concentrations in end-stage renal disease patients increase after
hemodialysis: Correlation with low molecular AGE adduct clearance.
Clin Chim Acta. 377(1-2), p213-20 (2007).
Gugliucci A, Mehlhaff K, Kinugasa E, Ogata H, Hermo R, Schulze J, Kimura S.
末期腎疾患(ESRD)患者においてAOPPは高値を示します。 |
| 7) |
Serum advanced oxidation protein products, myeloperoxidase and ascorbic acid in pre-eclampsia and eclampsia.
Aust N Z J Obstet Gynaecol. 46(6), p486-91 (2006).
Noyan T, Guler A, Sekeroglu MR, Kamaci M.
子癇患者ではマロンジアルデヒドが高値を示しますが、AOPPは有意差なし。 |
| 8) |
Impact of Angiotensin II Receptor Blocker on Plasma Levels of Adiponectin and Advanced
Oxidation Protein Products in Peritoneal Dialysis Patients.
Blood Purif. 24(5):445-450 (2006)
Furuya R, Odamaki M, Kumagai H, Hishida A.
腹膜透析患者では血漿AOPPは高値を示します。アギオテンシン2受容体ブロッカー(Candesartan) 投与により
血漿AOPPが低下します。 |
| 9) |
Association of metabolic syndrome risk factors with selected markers of oxidative status and
microinflammation in healthy omnivores and vegetarians.
Mol Nutr Food Res.50(9),p858-868(2006).
Sebekova K, Boor P, Valachovicova M, Blazicek P, Parrak V, Babinska K, Heidland A, Krajcovicova-Kudlackova M
メタボリックシンドロームとの関連性が報告されています。 |
| 10) |
Advanced oxidation protein products induce monocyte chemoattractant protein-1 expression
via p38 mitogen-activated protein kinase activation in rat vascular smooth muscle cells.
Chin Med J (Engl). 119(13):1088-93 (2006).
Peng KF, Wu XF, Zhao HW, Sun Y.
SDラット(雄)動脈由来の血管平滑筋細胞にAOPPを添加するとMCP-1のmRNAレベルが上昇します。 |
| 11) |
Protein oxidation status in patients with ankylosing spondylitis.
Pheumatlogy 43, p1235-1239 (2004)
C Yazici, K Kose, M Calis, S Kuzuguden and M Kirnap.
強直性脊椎炎(AS)においてAOPPは高値を示します。 |
| 12) |
Effects of exercise and training in hypoxia on antioxidant/pro-oxidant balance.
Eur J Clin Nutr. 60(12):1345-54 (2006).
Pialoux V, Mounier R, Ponsot E, Rock E, Mazur A, Dufour S, Richard R, Richalet JP, Coudert J, Fellmann N
低酸素条件下における運動で、AOPPが上昇することが報告されています。 |
| 13) |
Protein oxidation in obesity and insulin resistance.
Eur J Pediatr. 165(11),p753-756(2006)
Atabek ME, Keskin M, Yazici C, Kendirci M, Hatipoglu N, Koklu E, Kurtoglu S.
肥満、インシュリン抵抗性とAOPPとの関連性が報告されています。 |
| 14) |
Effect of white wine consumption on oxidative stress markers and homocysteine levels.
Physiol Res. 2006 Mar 23
Rajdl D, Racek J, Trefil L, Siala K
白ワイン摂取によりAOPPが低下することが報告されています。 |
| 15) |
Oxidative stress and inflammation in pregnancy.
Scand J Clin Lab Invest. 66(2),p121-127(2006)
Fialova L, Malbohan I, Kalousova M, Soukupova J, Krofta L, Stipek S, Zima T.
妊娠におけるAOPPの上昇が報告されています。 |
| 16) |
Advanced oxidation protein products accelerate atherosclerosis through
promoting oxidative stress and inflammation.
Arterioscler Thromb Vasc Biol. 26(5),p1156-1162(2006)
Liu SX, Hou FF, Guo ZJ, Nagai R, Zhang WR, Liu ZQ, Zhou ZM, Zhou M, Xie D, Wang GB, Zhang X.
高コレステロール血症ウサギを対象にウサギアルブミン酸化物(AOPP-RSA)を8週間静脈投与。
AOPP-RSA投与群では対照群に比べアテローム性動脈硬化病変が進行。 |
| 17) |
The structural and pharmacokinetic properties of oxidized human serum albumin,
advanced oxidation protein products (AOPP).
Drug Metab Pharmacokinet. 21(2), p140-146 (2006).
Iwao Y, Anraku M, Hiraike M, Kawai K, Nakajou K, Kai T, Suenaga A, Otagiri M.
血漿AOPPのクリアランスは主に肝臓と脾臓で行われることが報告されています。 |
| 18) |
Glycoxidation and inflammation in chronic haemodialysis patients.
Nephrol Dial Transplant 18, p2577-2581 (2003)
Marta Kalousova, Sylvie Sulkova, Lenka Fialova, Jirina Soukupova, Ivan Matous Malbohan, Pavel Spacek, Martin Braun,
Ludmila Mikulikova, Magdalena Fortova, Magdalena Horejsi, Vladimir Tesar and Tomas Zima
透析患者を対象とした血清AOPP測定例です。透析患者34名のAOPP平均値は144.3μmol/L(118.1-180)と、
健常者対照14名のAOPP平均値89.2μmol/L(76.2-96.6)に比べ有意に高値を示します。 |
| 19) |
Iron therapy, advanced oxidation protein products, and carotid artery intima-media thickness in end-stage renal disease.
Circulation 106, p2212-2217 (2002)
Tilman Drueke, Veronique Witko-Sarsat, Ziad Massy, Beatrice Descamps-Latscha, Alain P Guerin, Sylvain J Marchais,
Valerie Gausson and Gerard M London.
透析患者79名での測定で、AOPP濃度は149±41μmol/Lを示します。 |
| 20) |
Endotherial dysfunction and hypertention in 5/6 nephrectomized rats are mediated by vascular superoxide.
Kidney Internatioal 61, p586-590 (2002)
Galit Hasdan, Sydney Benchetrit, Gloria Rashid, Janice Green, Jacques Bernheim and Mauro Rathaus.
ラット血漿での測定例です。 |
| 21) |
The plasma concentration of advanced oxidation protein products and arterial stiffness in apparently healthy adults.
Free Radical Research 41(6), p645-649(2007)
Andrzej Wykretowicz, Karolina Adamska, Tomasz Krauze, Przemyslaw Guzik, Adam Szczepanik, Agnieszka Rutkowska, Henryk Wysoki
血漿AOPPは健常者において動脈硬化度に相関して高値を示すことが報告されています(R2 = 42%, p 0.0001)。 |
| 22) |
Advanced Oxidation Protein Products Activate Vascular Endothelial Cells via a RAGE-Mediated Signaling Pathway.
Antioxid. Redox Signal. 10(10), 2008
Zhi Jian Guo, Hong Xin Niu, Fan Fan Hou, Lu Zhang, Ning Fu, Ryoji Nagai, Xiao Lu, Bai Hong Chen, Yue Xin Shan,
Jian Wei Tian, Ram H. Nagaraj,Di Xie, and Xun Zhang
AOPPは糖尿病、慢性腎疾患、アテローム性動脈硬化病変における血管障害に関わっていることが知られています。
この文献ではAOPPがAGE受容体(RAGE)を介して血管内皮細胞を活性化しうることが示されています。 |
| 23) |
Comparative assessment of urinary oxidative indices in breast and colorectal cancer patients.
J Cancer Res Clin Oncol 135(2) p319-323 (2009)
S. Chandramathi, K. Suresh, Z. B. Anita and U. R. Kuppusamy
乳がん患者101名、大腸がん患者49名を対象に尿中AOPPを測定。
大腸がん患者および乳がん患者は健常対照に比べ尿中AOPPが有意に高値を示します。 |
| 24) |
Advanced Oxidation Protein Products Activate Intrarenal Renin?Angiotensin System via a CD36-Mediated, Redox-Dependent Pathway.
Antioxidants and Redox Signaling 00(0),p0-0 (2012) doi:10.1089/ars.2012.4603.
Wei Cao, Jie Xu, Zhan Mei Zhou, Guo Bao Wang, Fan Fan Hou, and Jing Nie.
AOPPがレニン-アンギオテンシン系を活性化することが示唆されています。 |
|
|
|
 |
| ビタミンC測定キット |
| No. |
【タイトル】 |
【内容】 |
| 1 |
ヒト血漿VCの正常値 |
4-15 mg/L (Burtis CA, Ashwood ER. Tietz textbook of clinical chemistry, 4th ed. Saunders:
Philadephia, 2006: 1107) ※出典により正常値、基準値は異なります。 |
| 2 |
ヒト以外の動物種 |
マウス、ラット、ウサギなど実験動物の血漿ビタミンCも測定可能です。
動物種や飼育条件等により検出限界以下となる可能性もありますのでご留意ください。 |
| 3 |
標準物質の性状について |
試薬性能向上のため、2008年より本製品の標準物質バイアルは、凍結乾燥パウダーが見えない構成と
なっております。使用説明書に記載されている通り、標準物質バイアルに蒸留水400μLを添加してご使用ください。 |
| 4 |
ビタミンC誘導体との反応性 |
本キットでは、アスコルビン酸のケト基を利用しています。このケト基がブロックされているような誘導体、
例えばリン酸 L-アスコルビルマグネシウムについては、本キットでは検出しないと考えられます。 |
| 5 |
血清・EDTA血漿での測定 |
本キットは血清サンプルにも適用可能です。
尚、EDTA血漿では測定できません。Li-heparin血漿または血清をご利用ください。 |
| 6 |
尿サンプルへの適用 |
本キットは尿サンプルにも適用可能です。予めサンプル希釈液で4倍希釈してから測定します。
詳細につきましては、使用説明書をご参照ください。 |
| 7 |
房水(眼球)にも適用できますか? |
測定できる可能性はあると考えられますが、現在のところ、房水への適用事例は把握しておりません。
ビタミンCは酸化を受けやすい物質ですので、サンプルの採取、保存の際にはなるべく短時間で低温条件下で
実施されることをお奨めします。保存はディープフリーザー(-80℃)、輸送の際はドライアイス充填を
お奨めします。 |
| 8 |
食品サンプルへの適用 |
食品サンプルへの適用事例はありません。
|
| 9 |
サンプルの保存方法 |
採血後は直ちに血漿/血清分離を行い、遮光下で冷蔵し24時間以内に測定してください。
保存する場合には凍結(-80℃を推奨)とし、なるべく早く測定してください。保存期間は80日以内とする報告があります。 |
| 10 |
コントロールバイアルの保存条件 |
製品改善のため、コントロールバイアルの保存条件が冷凍(-20℃)に変更されております。
納品時にパッケージが2個口に分かれておりますので、ご注意ください。尚、コントロールは
凍結乾燥品として製造されておりますので、短時間でしたら冷蔵〜室温下に置かれても
品質に問題ありません。 |
| 11 |
コントロールバイアルの溶解液量 |
使用説明書(19.08.2013版)において、CTRLバイアルの溶解液量について、p.16に500μL
との表記がありますが、正しくは250μLです(p.15および瓶ラベルの表記通りです)。 |
| 12 |
キット(冷蔵保存)を誤って
冷凍してしまったのですが? |
凍結してしまったキットの使用に関しましては、データがなく、
試薬性能に関する保証はできかねます。使用者のご判断により、お使いいただくことは可能ですが、
正しく測定できない場合もありますので、予めご了承ください。
|
| 13 |
A試薬に析出物が見られる場合 |
保管状況等により、稀に、試薬A(solution A)に針状の結晶が見られる場合があります。
製造元にて、測定値には問題ないことを確認しておりますが、ピペッティングの際、なるべく結晶を
吸い込まないよう、ご注意ください。軽く遠心して除去する方法もあります。
|
| 14 |
酸化型/還元型の検出について |
本キットはサンプル中のアスコルビン酸をデヒドロアスコルビン酸(酸化型)に変換したものを
比色法にて検出します。酸化型 + 還元型の総量を測定できますが、どちらか一方のみを検出することは
できません。
【参考情報】: アスコルビン酸(還元型ビタミンC)はHPLC法でも検出できます。HPLCをお持ちでしたら
試薬セット(KVC-290DL:KC2900)を用いて検出可能です。
詳細につきましては弊社
営業担当者(biotech@jaica.com)までお問合せください。
|
|
|
|
|
| 【参考文献】 |
| 1) |
Stability of whole blood and plasma ascorbic acid.
European Journal of Clinical Nutrition 61, p1233-1236(2007) A Karlsen, R Blomhoff and T E Gundersen.
血漿サンプルの採取および保存方法に関する文献です。アスコルビン酸は壊れやすいため、 採血後直ちに遠心分離し
-70℃にて保管(80日以内)します。 |
| 2) |
Pharmacokinetics of oral vitamin C.
Journal of Nutritional & Environmental Medicine, 17(3), p169-177(2008)
Stephen Hickey, Hilary J. Roberts, Nicholas J. Miller
高濃度のビタミンCはがん治療に役立つ可能性が指摘されています。ここではビタミンC経口投与における
血漿ビタミンC濃度の変動を検討しています。 |
| 3) |
Vitamin C treatment reduces elevated C-reactive protein.
Free Radical Biology and Medicine 46(1), p70-77 (2009)
Gladys Block, Christopher D. Jensen, Tapashi B. Dalvi, Edward P. Norkus, Mark Hudes, Patricia B. Crawford, Nina Holland,
Ellen B. Fung, Laurie Schumacher and Paul Harmatz
炎症マーカーである血漿CRP (C-reactive protein)が高い健常者を対象に、ビタミンC 1000mg/日を2ヶ月間投与すると
血漿CRP濃度がプラセボ群に比べ有意に低下することが報告されています。
一方、ビタミンE 800 IU/日の投与では有意差は認められませんでした。 |
| 4) |
Ascorbic acid combats arsenic-induced oxidative stress in mice liver.
Ecotoxicol Environ Saf. 72(2), p639-649 (2009)
Banerjee P, Bhattacharyya SS, Bhattacharjee N, Pathak S, Boujedaini N, Belon P, Khuda-Bukhsh AR.
マウスにおいて、ビタミンCは砒素による肝臓毒性からの保護作用を示すことが報告されています。 |
| 5) |
Vitamin C Intake and the Risk of Gout in Men. A Prospective Study.
Arch Intern Med 169(5), p502-507 (2009), Hyon K. Choi, Xiang Gao, Gary Curhan.
男性46994名を対象とした20年間にわたるプロスペクティブスタディ。ビタミンCサプリメントの摂取は痛風発症リスクを
有意に低下させることが報告されています。ビタミンCサプリメントを摂取しない人に比べ、ビタミンCサプリメント1500mg/日以上摂取する人の
痛風発症の相対リスクは、0.55であり、用量依存的に発症リスクが低下します。 |
| 6) |
Pharmacologic concentrations of ascorbate are achieved by parenteral administration and exhibit
antitumoral effects.
Free Radical Biology and Medicine 47(1), p32-40 (2009)
Julien Verrax and Pedro Buc Calderon
高濃度のビタミンCは広範囲の種類のがん細胞を死滅させること(EC50は3〜7mM)、ビタミンCの静脈注射により
血中濃度を20mMまで上げることができることが報告されています。マウス肝がんを使った試験ではビタミンCの静脈注射ではがんの成長抑制作用が
観察されましたが、経口投与では効果が認められませんでした。 |
|
|
|
 |
| 血清ミエロペルオキシダーゼ(MPO)測定キット:ELISA法 |
| No. |
【タイトル】 |
【内容】 |
| 1 |
Q:実験動物でも測定できますか? |
A:本キットは、ヒト ミエロペルオキシダーゼに特異的な抗体を使用しております。
ヒト以外への適用は難しいと考えられます。 |
| 2 |
Q:保健適用されているMPO-ANCAとの違いは何ですか? |
A:MPO-ANCA(抗好中球細胞質抗体)とはミエロペルオキシダーゼ(MPO)に対する
自己抗体を指します。本キットは、抗MPO自己抗体ではなく、サンプル中のMPOを検出します。
また、本キットは研究用試薬であり、診断/治療等に 用いることはできません。 |
| 3 |
Q:血清、血漿以外のサンプルに適用できますか? |
A:尿、糞便、唾液中のMPOを測定できるキットが別途ございます。
ご注文の際は尿中MPO測定キット(製品コードKMP-100D)とご指定ください。
また、組織サンプルや培養上清には、血清MPO測定キットよりも、尿中MPO測定キットを推奨します。
|
| 4 |
Q:血清、血漿サンプルの保存期間 |
A:-80℃にて1年間保存可能です。
|
|
|
|
|
| 【参考文献】 |
| 1) |
Pathological uterine perfusion in the second trimester is not associated with neutrophil activation.
Hypertens Pregnancy. 22(3), p239-245.(2003)
Stepan H, Heihoff-Klose A, Faber R.
本キットを使用した研究例です。 |
| 2) |
Myeloperoxidase and protein oxidation in the airways of young children with cystic fibrosis.
Am J Respir Crit Care Med 170(12),p1317-1323(2004)
Kettle AJ, Chan T, Osberg I, Senthilmohan R, Chapman AL, Mocatta TJ, Wagener JS
嚢胞性繊維症患者(小児23名)において気管支肺胞洗浄液(BALF)中のカルボニル化蛋白(0.94 nmol/mg protein)は
健常対照(0.40 nmol/mg protein)に比べ有意に高値を示します。 |
| 3) |
Validation of the human ozone challenge model as a tool for assessing anti-inflammatory drugs
in early development.
J Clin Pharmacol.45(5), p498-503 (2005)
Holz O, Tal-Singer R, Kanniess F, Simpson KJ, Gibson A, Vessey RS, Janicki S, Magnussen H, Jorres RA, Richter K.
本キットを使用した研究例です。 |
| 4) |
Myeloperoxidase predicts progression of carotid stenosis in states of low high-density lipoprotein
cholesterol.
J Am Coll Cardiol. 47(11),p2212-2218.(2006)
Exner M, Minar E, Mlekusch W, Sabeti S, Amighi J, Lalouschek W, Maurer G, Bieglmayer C, Kieweg H, Wagner O, Schillinger M.
本キットを使用した研究例です。 |
| 5) |
Myeloperoxidase serves as a marker of oxidative stress during single haemodialysis session using
two different biocompatible dialysis membranes.
Nephrol Dial Transplant. 20(6), p1134-1139 (2005)
Wu CC, Chen JS, Wu WM, Liao TN, Chu P, Lin SH, Chuang CH, Lin YF.
透析患者において血漿ミエロペルオキシダーゼ(MPO活性)が上昇すること、他の酸化ストレスマーカー
(血清8-OHdG、AOPP)が
亢進することが報告されています。 |
| 6) |
Angiotensin type-1 receptor A1166C gene polymorphism correlates with oxidative stress levels in
human heart failure.
Hypertension 47(6),p1155-1161(2006)
Cameron VA, Mocatta TJ, Pilbrow AP, Frampton CM, Troughton RW, Richards AM, Winterbourn CC.
心不全患者127名および健常対照112名を対象に血漿ミエロペルオキシダーゼ(MPO)を測定。心不全患者の血漿MPO濃度
(51 ng/mL)は健常対照(37 ng/mL)に比べ高値を示します。また、心不全患者における1型アンギオテンシン受容体(AT1R)のA1166C多型によって
MPO濃度が異なることが見出されており、CC(72 ng/mL)はAC(52 ng/mL)およびAA(39 ng/mL)に比べ有意に高値を示します。 |
| 7) |
Plasma concentrations of myeloperoxidase predict mortality after myocardial infarction.
J Am Coll Cardiol. 49(20), p1993-2000 (2007)
Mocatta TJ, Pilbrow AP, Cameron VA, Senthilmohan R, Frampton CM, Richards AM, Winterbourn CC.
急性心筋梗塞患者512名および対照群156名を対象に血漿MPOを測定し、患者の死亡率を5年間追跡調査。
急性心筋梗塞患者の入院24〜96時間における血漿ミエロペルオキシダーゼ(MPO: 55 ng/mL)は対照群(39ng/m)に比べ有意に高値を示し、
MPOが平均レベル以上であることは死亡率の独立した予測因子(オッズ1.8、p=0.034)であることが報告されています。
また、同時に蛋白質の酸化損傷マーカーである、カルボニル化蛋白の測定も行われており、
急性心筋梗塞患者において血漿中のカルボニル化蛋白が有意に高値を示すことが
示されています。 |
|
|
|
 |
| 尿中ミエロペルオキシダーゼ(MPO)測定キット:ELISA法 |
| No. |
【タイトル】 |
【内容】 |
| 1 |
Q:血清MPO測定キットとの違い |
A:本キットの主な測定対象は、ヒト尿および便です。 |
| 2 |
参考値 |
ヒト糞便: 2000 ng/g以下 |
| 3 |
組織MPOの測定方法 |
本キットは、組織ホモジネートへの適用が可能です。
1) 組織サンプルを液体窒素中で凍結、超音波ホモジナイザーを使って破砕します。
2) 1% Triton X-100を含む 1mL リン酸バッファー(0.14 M NaCl, 2.6 mM KCl, 8 mM Na2HPO4, 1.4mM KH2PO4, pH7.4)
にてホモジナイズします。
3) 100,000Gにて1時間超遠心し、上清中のタンパク濃度を測定します。
4) MPO測定キットに適用します。 |
| 4 |
培養上清への適用 |
本キットを使って、培養上清中のMPOを測定できる可能性があります。
培養前の培地と比較する形で測定します。培地の組成により、希釈率の検討が必要となる場合があります。
具体的な文献、測定値はありません。 |
|
|
|
|
| 【参考文献】 |
| 1) |
Myeloperoxidase concentrations in the stool as a new parameter of inflammatory bowel disease.
Kurume Med J. 45(1),p69-73 (1998).Saiki T. |
|
|
|
 |
| ヒト酸化LDL 測定キット |
| No. |
【タイトル】 |
【内容】 |
| 1 |
調製した試薬の安定性 |
スタンダード、コントロール試薬は測定当日に調製してください。溶解したスタンダード、コントロール、
希釈済みのコンジュゲート試薬は不安定であり保存できません。 |
| 2 |
血清/血漿サンプルの取扱い |
本キットでは、血清、EDTA血漿、ヘパリン血漿を測定できます。サンプルの保存は-20℃以下としてください。
乳び、溶血のあるサンプルでは測定できません。特に血漿の場合、不溶物が含まれている場合には遠心(10000g*5分)して
取り除いてから測定してください。EDTA血漿、血清サンプルはサンプル希釈液にて10倍希釈してから
測定することをお奨めします。
EDTA血漿につきましては、開発元ではEDTA-3Kにて検証しており、EDTA-2Na,2Kは未検証です。 |
| 3 |
血清と血漿の相関性 |
血清検体と、同一被験者由来の血漿検体中の酸化LDL濃度は、ほぼ同等の値を示します。
(相関係数 r2=0.998 社内データ) |
| 4 |
検体の保存安定性 |
-80℃凍結にて1年間安定です。1〜2回程度の凍結融解は問題ありません。 |
| 5 |
参考値 |
健常者120名の血漿/血清を測定したとき、酸化LDL濃度は 95.32±37.85 ng/mLとの
測定結果が得られています(開発製造元の社内データ)。また、2型糖尿病患者86名を対象とした試験では
142.37±49.84 ng/mLであり、健常者群に対し有意に高値を示します。 |
| 6 |
プレートに固相化されている抗体 |
酸化LDLは、多様な酸化修飾物で
構成されており、ELISA法の検出特性は使用されている抗体の特異性に依存します。酸化LDLのELISAキットに使用されている
抗体には、抗MDA-LDL抗体、抗AGE-LDL抗体、抗CML-LDL抗体、抗-酸化ホスファチジルコリン-LDL抗体、抗Cu酸化LDL抗体等が
知られております。本キットでは"MDA-modified apolipoprotein-100"に対する抗体が固相化されています。
参考文献: Development of capture assays for different modifications of human low-density lipoprotein.
Clin Diagn Lab Immunol 12(1)p68-75(2005).
Virella G, Derrick MB, Pate V, Chassereau C, Thorpe SR, Lopes-Virella MF. |
| 7 |
尿を測定できますか? |
具体的なデータはありませんが、少なくとも健常者尿では、
検出できない可能性が高いと考えられます。
測定を試みられる場合には、夾雑因子の影響を避けるため3倍以上に希釈してください。 |
|
|
|
|
| 【参考文献】 |
| 1) |
Oxidated low-density lipoproteins (oxLDL) and peroxides in plasma of Down syndrome patients.
Arch Gerontol Geriatr. 44(Suppl 1),p225-232(2007)
Licastro F, Dogliotti G, Goi G, Malavazos AE, Chiappelli M, Corsi MM.
本キットを使用した測定例です。小児および成人のダウン症患者では血漿中の酸化LDL濃度が対照群に比べ高値を
示します。
|
| 2) |
Hyperhomocysteinemia and elevated ox-LDL in Tunisian type 2 diabetic patients: role of genetic and
dietary factors. Clin Biochem. 40(13-14),p1007-1014(2007)
Koubaa N, Nakbi A, Smaoui M, Abid N, Chaaba R, Abid M, Hammami M.
2型糖尿病患者を対象に、本キットを使用した研究例です。
|
|
|
|
| ヒト酸化LDL 自己抗体測定用ELISAキット |
| No. |
【タイトル】 |
【内容】 |
| 1 |
納期と有効期限について |
本キットは受注生産品のため、納期はご注文いただいてから3週間〜1ヶ月程度となります。
製造後の納期は6ヶ月です。 |
|
|
|
|
| 【参考文献】 |
| 1) |
Circulating autoantibodies to oxidized LDL correlate with impaired coronary endothelial function
after cardiac transplantation.
Arterioscler Thromb Vasc Biol 22(12), p2044-2048 (2002). Fang JC, Kinlay S, Behrendt D, Hikita H, Witztum JL, Selwyn AP, Ganz P.
|
| 2) |
Clinical significance of antibodies against oxidised low density lipoprotein in early RA.
Ann Rheum Dis 55(8), p558-559(1996). Paimela L, Helve T, Leirisalo-Repo M, Vaarala O, Alfthan G, Palosuo T, Aho K.
関節リウマチ患者における3年間の追跡調査の結果、酸化LDL自己抗体力価は、抗リウマチ薬投与により
低下することが報告されています。
|
|
|
|
| グルタチオンS-トランスフェラーゼπ測定キット |
| No. |
【タイトル】 |
【内容】 |
| 1 |
GST-P1単量体との反応性 |
GST-πはGST-P1サブユニットの2量体で構成されています。本キットはGST-πおよびGST-P1(単量体)の
どちらでも認識します。リコンビナントとの反応性につきましては知られておりません。
|
|
|
|
|
| 【参考文献】 |
| 1) |
Quantitation of glutathione transferase-pi in the urine by radioimmunoassay.
Nephron.66(2):162-169(1994)
Sundberg AG, Appelkvist EL, Backman L, Dallner G.
|
| 2) |
Urinary pi-class glutathione transferase as an indicator of tubular damage in the human kidney.
Nephron. 67(3):308-316(1994)
Sundberg AG, Appelkvist EL, Backman L, Dallner G.
|
| 3) |
Novel Role for Glutathione S-Transferase pi:
REGULATOR OF PROTEIN S-GLUTATHIONYLATION FOLLOWING OXIDATIVE AND NITROSATIVE STRESS.
J. Biol. Chem. 284(1), p436-445 (2009)
Danyelle M. Townsend, Yefim Manevich, Lin He, Steven Hutchens, Christopher J. Pazoles, and Kenneth D. Tew
酸化ストレス及びNOストレス下におけるタンパク質S-グルタチオニル化にはGST酵素活性が
必要であることが示されています。
|
| 4) |
Glutathione S-transferase π localizes in mitochondria and protects against oxidative stress.
Free Radical Biology and Medicine 46(10), p1392-1403 (2009)
Shinji Goto, Miho Kawakatsu, Shin-ichi Izumi, Yoshishige Urata, Kan Kageyama, Yoshito Ihara, Takehiko Koji and Takahito Kondo
グルタチオン-S-トランスフェラーゼπ(GST-π)がミトコンドリア内に移行し、ミトコンドリアにおける酸化ストレスからの
保護に関わっていることが示唆されています。
|
|
|
|
 |
| PMNエラスターゼ測定キット |
| No. |
【タイトル】 |
【内容】 |
| 1 |
血清サンプル採取/保存の注意点 |
採血後は1時間以内に遠心し、血清分離を行います。当日測定しない場合には-20℃にて凍結保存します。
乳びおよび溶血検体には適用できません。血清サンプルは、凍結融解による変動は観察されませんが、血漿サンプルでは
凍結融解の繰り返しや、採血から測定までの経過時間によって測定値の変動が見られる場合があります。血漿サンプルを
用いる場合には、採血から測定までの条件を一定にする必要があります。
また、血清中のエラスターゼ濃度は、血漿に比べ10倍程度高値となることが知られています。これは、血液凝固の過程で
顆粒球が活性化され、エラスターゼが放出されるためと考えられています。
|
| 2 |
参考値 |
健常者(便): 62 ng/mL以下
健常者(血漿): 19〜78 ng/mL
健常者(血清): 186〜1991 ng/mL(平均値 688 ng/mL)
|
|
|
| ご質問などお気軽にどうぞ(メール) |
| 抗Nε-(carboxymethyl)lysine: CML抗体 |
| No. |
【タイトル】 |
【内容】 |
| 1 |
直接ELISA法による検出 |
蛋白質に結合したCMLは直接ELISA法にて検出できる場合があります。
1) 対象となる蛋白質 5μg/100μLをマイクロプレートにコート。
2) ブロッキング
3) 1000倍希釈した抗CML抗体を100μL/well分注し、室温にて2時間静置。
4) 洗浄し、HRP標識-抗ウサギIgGを100μL/well分注し、室温にて2時間静置。
5) 洗浄し、TMBZ溶液により発色。450nmの吸光度を測定。
参考文献:J Clin Invest. 99(3), p457-468(1997)
|
|
|
|
|
| 【参考文献】 |
| 1) |
Increased accumulation of the glycoxidation product N(epsilon)-(carboxymethyl)lysine in human
tissues in diabetes and aging.
Schleicher ED, Wagner E, Nerlich AG., J Clin Invest. 99(3), p457-468(1997)
ELISAによるCML測定方法、免疫組織染色による検出が紹介されています。
|
|
|
|
| チオールステータス測定キット |
| No. |
【タイトル】 |
【内容】 |
| 1 |
ヒト以外の動物種への適用について |
・大腸菌:適用事例はありません。
・マウス血清:具体的な適用例はありませんが、適用できる可能性があります。ただ、測定レンジ内に
収まるかどうかは、実施してみないと分かりません。ぜひお試しください。
|
| 2 |
血漿分離の際の温度 |
血漿分離の遠心は4°Cが好ましいとされています。
|
| 3 |
サンプルの保存安定性 |
-20°Cにて1ヶ月、-80°Cにて3ヶ月安定です。凍結融解は避けてください。
|
| 4 |
測定原理について |
本キットはEllman's methodに基づいています。
|
|
|
|
|
| 【参考文献】 |
| 1) |
Reduced level of serum thiols in patients with a diagnosis of active disease.
J Anti Aging Med 6(4),p327-334(2003). Banne AF, Amiri A, Pero RW.
|
| 2) |
Oxygen free radicals and congestive heart failure.
Br Heart J 65(5),p245-248(1991). Belch JJ, Bridges AB, Scott N, Chopra M.
|
| 3) |
Oxidative stress. An early phenomenon characteristic of acute experimental pancreatitis.
Int J Pancreatol 12(3),p193-199(1992). Dabrowski A, Gabryelewicz A.
|
| 4) |
A precise method for the determination of whole blood and plasma sulfhydryl groups.
Anal Biochem 93(1),p98-102(1979). Ellman G, Lysko H.
|
| 5) |
Measurement of protein thiol groups and glutathione in plasma.
Methods Enzymol 233,p380-385(1994). Hu ML.
|
| 6) |
Spectrophotometric assay of thiols. Methods Enzymol 143,p44-67(1987). Jocelyn PC.
|
| 7) |
Reduced free-radical-trapping capacity and altered plasma antioxidant status in cystic fibrosis.
Pediatr Res 33(3),p247-250(1993). Langley SC, Brown RK, Kelly FJ.
|
| 8) |
Elevated levels of xanthine oxidase in serum of patients with inflammatory and autoimmune rheumatic
diseases.
Inflammation 17(5),p551-561(1993). Miesel R, Zuber M.
|
| 9) |
Free radical activity and loss of plasma antioxidants, vitamin E, and sulfhydryl groups in patients
with burns: the 1993 Moyer Award.
J Burn Care Rehabil 14(6),p602-609(1993). Nguyen TT, Cox CS, Traber DL, Gasser H, Redl H, Schlag G, Herndon DN.
|
| 10) |
Reassessment of Ellman's reagent. Methods Enzymol 91,p49-60(1983). Riddles PW, Blakeley RL, Zerner B.
|
| 11) |
Serum and synovial fluid histidine: a comparison in rheumatoid arthritis and osteoarthritis.
Rheumatol Int 6(6),p251-254(1986). Sitton NG, Dixon JS, Bird HA, Wright V.
|
|
|
|
 |
| ヒト ミオスタチン(Myostatin/GDF-8)測定キット:ELISA法 |
| No. |
【タイトル】 |
【内容】 |
| 1 |
調製した試薬の保存安定性 |
洗浄バッファー: 調製後冷蔵にて1ヶ月以内
ビオチン標識ミオスタチン(Tracer試薬): 希釈した溶液は不安定であり、保存できません
スタンダード: 再構成した溶液は、不安定であり、保存できません
コントロール: 再構成した溶液は、不安定であり、保存できません |
| 2 |
吸光度が2を超えた場合 |
測定波長を450nmから405nmに変更して、測定を試みてください。 |
| 3 |
検量線の近似関数 |
4-パラメータ-アルゴリズム(縦軸:吸光度-真数/横軸:濃度-対数)を推奨します。
また折れ線(隣接する検量点間を直線で近似)も使用可能です。
お手持ちの検量線の計算ソフトがないようでしたら、弊社までExcel形式にて吸光度データを
お送りください。
折り返し計算結果をお送りさせていただきます。尚、ご返事まで数日かかる場合があります。予めご了承ください。 |
| 4 |
本キットの仕様変更について |
製品改良のため、2012年11月に製造元において仕様変更が行われております。
ご使用の前に、製品に同梱されている使用説明書を必ずご確認ください。
|
| 5 |
サンプルの保存条件 |
サンプル(EDTA血漿または血清)は-20℃以下にて凍結保存してください。
|
| 6 |
プレートの取扱い |
プレートは12x8の分割式となっており、必要に応じて分割使用ができます。
使用状況により外れやすくなるようでしたら、上下端をテープ等で固定すると、
より扱いやすくなります。
|
| 7 |
受託検査について |
本キットを用いた分析は受託研究としてお引き受け可能です。
受託条件等につきましては、受託研究発注書を
ご覧ください。
費用はヒト血清/血漿 28検体あたり288,000円(税抜)です。
詳細は、弊社 受託研究担当者までお問い合わせください。
|
|
|
|
|
| 【参考文献】 |
| 1) |
Regulation of skeletal muscle mass in mice by a new TGF-beta superfamily member.
Nature 387(6628),p83-90(1997). McPherron AC, Lawler AM, Lee SJ.
ミオスタチン(GDF-8)遺伝子の同定、発現部位、ノックアウトでの表現型に関する報告です。
|
| 2) |
Muscle-bone interactions, revisited. Bone 27(3),p339-340(2000). Turner CH.
|
| 3) |
Serum myostatin-immunoreactive protein is increased in 60-92 year old women and men with muscle
wasting.
J Nutr Health Aging 6(5),p343-348(2002). Yarasheski KE, Bhasin S, Sinha-Hikim I, Pak-Loduca J, Gonzalez-Cadavid NF.
血清ミオスタチン濃度が、加齢による筋肉減少(サルコペニア)の指標となることが示唆されています。
|
| 4) |
Organization of the human myostatin gene and expression in healthy men and HIV-infected men with
muscle wasting.
Proc Natl Acad Sci USA 95(25),p14938-14943(1998).
Gonzalez-Cadavid NF, Taylor WE, Yarasheski K, Sinha-Hikim I, Ma K, Ezzat S, Shen R, Lalani R, Asa S, Mamita M, Nair G, Arver S, Bhasin S.
成人健常者におけるミオスタチンレベルは、除脂肪体重と負の相関性を示すこと、HIV陽性患者ではミオスタチン濃度が
高値を示すことが報告されています。
|
| 5) |
Resistance to body fat gain in 'double-muscled' mice fed a high-fat diet.
Int J Obes (Lond) 30(5),p868-870(2006). Hamrick MW, Pennington C, Webb CN, Isales CM.
ミオスタチン ノックアウトマウスでは、高脂肪食を投与しても肥満にならないことが観察されています。
|
| 6) |
Plasma myostatin-immunoreactive protein is increased after prolonged bed rest with low-dose T3
administration.
J Gravit Physiol 6(2),p11-15(1999). Zachwieja JJ, Smith SR, Sinha-Hikim I, Gonzalez-Cadavid N, Bhasin S.
T3の50μg/日投与下にて健常男性を25日間安静に保つと、筋肉量減少、血漿ミオスタチンが12%上昇します。
|
| 7) |
Myostatin: a therapeutic target for skeletal muscle wasting.
Curr Opin Clin Nutr Metab Care 7(3),p259-263(2004). Roth SM, Walsh S.
抗ミオスタチン抗体の医薬品への応用に関する解説です。
|
| 8) |
Energy Balance, Myostatin, and GILZ: Factors Regulating Adipocyte Differentiation in Belly and Bone.
PPAR Res 92501(2007). Shi X, Hamrick M, Isales CM.
|
| 9) |
Transgenic expression of myostatin propeptide prevents diet-induced obesity and insulin resistance.
Biochem Biophys Res Commun 337(1),p248-255(2005). Zhao B, Wall RJ, Yang J.
マウスにおいてミオスタチンプロペプチド導入によりミオスタチンの機能をブロックすると、野生型に比べ筋肉量が45〜115%
増えること、高脂肪食摂取下でも血糖値、体脂肪、インシュリン感受性が維持されることが報告されています。
|
| 10) |
Myostatin decreases with aerobic exercise and associates with insulin resistance.
Med Sci Sports Exerc 42(11),p2023-2029(2010). Hittel DS, Axelson M, Sarna N, Shearer J, Huffman KM, Kraus WE.
中年男性(平均53歳)における有酸素運動(1200kcal/週 x 6ヶ月)は筋肉組織および血漿中のミオスタチン濃度を
20%低下させるとともに、インシュリン感受性を改善することが報告されています。
|
| 11) |
Cellular markers of muscle atrophy in chronic obstructive pulmonary disease.
Am J Respir Cell Mol Biol 42(4),p461-471(2010).
Plant PJ, Brooks D, Faughnan M, Bayley T, Bain J, Singer L, Correa J, Pearce D, Binnie M, Batt J.
COPD(慢性閉塞性肺疾患)患者では、筋肉組織におけるミオスタチン発現レベルが健常者対照に比べ有意に高いことが報告されています。
|
|
|
|
 |
| 血漿ニトロチロシン測定キット |
| No. |
【タイトル】 |
【内容】 |
| 1 |
NWLSS社製品との違いについて |
弊社が取り扱っておりますニトロチロシン測定キットには、下記の3種類があります。
・KNT-150D 血漿ニトロチロシン測定キット (本製品)
・KNT-029DT ヒト血漿ニトロチロシン測定キット
・KNT-002W ニトロチロシン測定キット
ここでは血漿ニトロチロシン測定キットに関する技術情報をご紹介しております。上記3種類のキットは
メーカー、仕様が異なっていることから、検出特性(測定値、相関性など)が異なる場合がありますのでご留意ください。
尚、KNT-002W ニトロチロシン測定キットの技術情報に関しましては、
こちらをご参照ください。
|
| 2 |
動物への適用について |
ニトロチロシンは構造上、種依存性がありません。本キットはヒト以外の動物にも適用可能です。
|
| 3 |
便サンプルへの適用について |
抽出処理を行うことで、便サンプルにも適用可能です。抽出プロトコルの詳細につきましては
使用説明書をご参照ください。
|
| 4 |
ヒト血清の測定例 |
本キットによる健常者血清(N=78)測定値は、平均 207 nM(48〜1533 nMに分布)です。
出典:メーカー使用説明書
|
| 5 |
尿サンプルへの適用について |
現在のところ報告例はありません。
|
| 6 |
培養細胞への適用について |
現在のところ具体的な測定例は把握しておりませんが、細胞中に十分量存在していれば
検出できる可能性があります。
|
| 7 |
キットの仕様変更について
(2012年12月) |
製造元での仕様変更に伴い、商品コードが旧製品(KNT-034DT)から新製品(KNT-150D)に
変更となっております。尚、ヒト血清を新旧キットで測定したときの相関係数はr=0.99です。
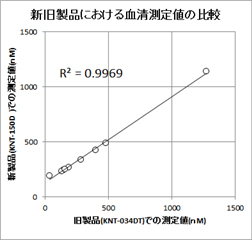
|
| 8 |
サンプルの保存安定性 |
-20℃凍結保存では6ヶ月、-80℃では1年程度安定とされています。
|
|
|
|
|
| 【参考文献】 |
| 1) |
Gonsette RE.; Neurodegeneration in multiple sclerosis: the role of oxidative stress and excitotoxicity.
J Neurol Sci. 274(1-2), p48-53 (2008)
|
| 2) |
Ischiropoulos H. ; Protein tyrosine nitration - an update. Arch Biochem Biophys. 484(2), p117-121 (2009)
|
| 3) |
Peluffo G, Radi R.; Biochemistry of protein tyrosine nitration in cardiovascular pathology.
Cardiovasc Res. 75(2), p291-302 (2007)
|
| 4) |
Souza JM, Peluffo G, Radi R.; Protein tyrosine nitration--functional alteration or just a biomarker?
Free Radic Biol Med. 45(4), 357-366 (2008)
|
|
|
|
| カルボニル化蛋白測定キット(ヒト/動物用) |
| No. |
【タイトル】 |
【内容】 |
| 1 |
調製後の試薬の安定性 |
希釈済み洗浄液(WASHBUF)は冷蔵(2-8℃)にて1ヶ月間保存できます。
希釈済み1次抗体試薬(AB)は冷蔵(2-8℃)にて2日間保存できます。
|
| 2 |
サンプルの保存安定性 |
サンプルの輸送時には必ず冷却してください。室温では24時間安定です
(ただし微生物の繁殖にご注意ください)。
|
| 3 |
限外濾過処理は何のために
実施するのですか? |
サンプル中のタンパク質をDNPH試薬で誘導体化する際、カルボニル基を含む他の成分
(アスコルビン酸や核酸など)も同時に誘導体化されます。こうした夾雑物の多くはタンパク質に比べ
低分子であることから、限外濾過フィルターで除去することができます。
|
| 4 |
限外濾過フィルターは専用のもの
(商品コード:KPC-FLT)でなくては
なりませんか? |
メーカーで検証済みであることから、専用の限外濾過フィルターの使用をお勧めします。
もし、やむを得ない場合には、分画分子量10kDaの限外濾過フィルターをお試しください。
専用フィルターのサイズは直径10.8mm、高さ49.9mm、分画分子量は10kDa、容量は0.5mL、
最小最終濃縮量は15μLです。
|
| 5 |
他のキットとの相関性について |
他のカルボニル化蛋白測定キット(KPC-010BT、KPC-780DT)との比較データはありません。
|
| 6 |
参考値 |
ヒトEDTA血漿: 75〜200pmol/mgに分布 (出典:製品同梱の使用説明書)
|
| 7 |
動物由来サンプルへの適用 |
本キットはウサギを除く全ての動物種に適用可能です。
ウサギに適用できない理由は、検出にウサギ由来抗体を使用しているためです。
|
| 8 |
組織サンプルにはBHTを添加 |
組織サンプルのホモジネートを調製する際には、酸化防止のため、BHTの添加を推奨します。
例えばBHTストック液 4mM/EtOHを、1/100容量添加して40μMとします。ホモジネートの調製には
氷冷PBS等が用いられます。
|
|
|
|
|
| 【参考文献】 |
| 1 |
Oxidatively modified proteins in aging and disease. Beal MF.
Free Radic Biol Med. 32(9), p797-803 (2002)
|
| 2) |
Protein oxidation in aging, disease, and oxidative stress. Berlett BS, Stadtman ER.
J Biol Chem 272(33),p20313-20316(1997)
|
| 3) |
Protein carbonyl measurement by a sensitive ELISA method.
Buss H, Chan TP, Sluis KB, Domigan NM, Winterbourn CC. Free Radic Biol Med 23(3),p361-366(1997).
|
| 4) |
Protein oxidation and aging. I. Difficulties in measuring reactive protein carbonyls in
tissues using 2,4-dinitrophenylhydrazine. Cao G, Cutler RG. Arch Biochem Biophys 320(1),p106-114(1995).
|
| 5) |
Protein damage and degradation by oxygen radicals. III. Modification of secondary and tertiary
structure. Davies KJ, Delsignore ME. J Biol Chem 262(20),p9908-9913(1987)
|
| 6) |
Biochemistry and pathology of radical-mediated protein oxidation.
Dean RT, Fu S, Stocker R, Davies MJ. Biochem J 324 (Pt 1),p1-18(1997)
|
| 7) |
Dialysis-induced oxidative stress: biological aspects, clinical consequences, and therapy.
Descamps-Latscha B, Drueke T, Witko-Sarsat V. Semin Dial 14(3),p193-199(2001)
|
| 8) |
Protein damage and inflammation in uraemia and dialysis patients.
Galli F. Nephrol Dial Transplant. 22(5),v20-36(2007)
|
| 9) |
Oxidation of proteins in neonatal lungs.
Gladstone IM Jr, Levine RL. Pediatrics 93(5),p764-768(1994)
|
| 10) |
Oxidatively modified proteins in bronchoalveolar lavage fluid of patients with ARDS and patients
at-risk for ARDS. Lenz AG, Jorens PG, Meyer B, De Backer W, Van Overveld F, Bossaert L, Maier KL.
Eur Respir J 13(1),p169-174(1999)
|
| 11) |
Carbonyl modified proteins in cellular regulation, aging, and disease.
Levine RL. Free Radic Biol Med 32(9),p790-796(2002)
|
| 12) |
Oxidative modification of proteins during aging.
Levine RL, Stadtman ER. Exp Gerontol 36(9),p1495-1502(2001)
|
| 13) |
Endogenous generation of reactive oxidants and electrophiles and their reactions with DNA
and protein. Marnett LJ, Riggins JN, West JD. J Clin Invest 111(5),p583-593(2003)
|
| 14) |
The impact of preoperative micronutrient supplementation in lung surgery. A prospective
randomized trial of oral supplementation of combined alpha-ketoglutaric acid and 5-hydroxymethylfurfural.
Matzi V, Lindenmann J, Muench A, Greilberger J, Juan H, Wintersteiger R, Maier A, Smolle-Juettner FM.
Eur J Cardiothorac Surg 32(5),p776-782(2007)
|
| 15) |
Modification of plasma proteins by cigarette smoke as measured by protein carbonyl formation.
Reznick AZ, Cross CE, Hu ML, Suzuki YJ, Khwaja S, Safadi A, Motchnik PA, Packer L, Halliwell B.
Biochem J 286 (Pt 2),p607-611(1992)
|
| 16) |
Excess brain protein oxidation and enzyme dysfunction in normal aging and in Alzheimer disease.
Smith CD, Carney JM, Starke-Reed PE, Oliver CN, Stadtman ER, Floyd RA, Markesbery WR.
Proc Natl Acad Sci U S A 88(23),p10540-10543(1991)
|
| 17) |
Metal-catalyzed oxidation of proteins. Physiological consequences.
Stadtman ER, Oliver CN. J Biol Chem 266(4),p2005-2008(1991).
|
| 18) |
Protein oxidation and proteolysis during aging and oxidative stress.
Starke-Reed PE, Oliver CN. Arch Biochem Biophys 275(2),p559-567(1989)
|
| 19) |
Damage to DNA by reactive oxygen and nitrogen species: role in inflammatory disease and
progression to cancer. Wiseman H, Halliwell B. Biochem J 313 (Pt 1),p17-29(1996)
|
| 20) |
Peroxiredoxin 6 fails to limit phospholipid peroxidation in lung from Cftr-knockout
mice subjected to oxidative challenge. Trudel S, Kelly M, Fritsch J, Nguyen-Khoa T, Therond P, Couturier M, Dadlez M,
Debski J, Touqui L, Vallee B, Ollero M, Edelman A, Brouillard F.
PLoS One 4(6):e6075 (2009) doi: 10.1371/journal.pone.0006075.
マウス臓器における本キットの適用例です
|
|
|
|
 |
| ヒト血清 カルボニル化蛋白測定キット |
| No. |
【タイトル】 |
【内容】 |
| 1 |
他のキットとの相関性について |
他のカルボニル化蛋白測定キットとの比較データはありません。
|
| 2 |
サンプルの保存期間について |
ヒト血清サンプルは、-80℃にて3ヵ月間保存可能です。
|
|
|
|
|
Copyright ©
JaICA. All rights reserved.
|

